Nästan alla, 80–90 procent, som har typ 2-diabetes är överviktiga eller har fetma men bara cirka en tiondel av de som är överviktiga har typ 2-diabetes.
Varför förblir vissa friska trots sin fetma, vad går snett hos dem som blir sjuka och vad är det som skiljer metabolt hälsosamt fett från det ohälsosamma? Det är frågor som fettforskaren Olga Göransson vill ha svar på.
Det finns flera olika hypoteser kring vilka fel i fettvävnaden som orsakar sjukdom vid fetma, och även kring hur dessa fel uppstår. Vid fetma ser man ofta en låggradig inflammation i fettvävnaden vilket skulle kunna bidra till uppkomsten av insulinresistens och eftersom fettvävnaden också är ett hormonproducerande organ skulle även den rubbade hormonbalansen som ses vid fetma kunna påverka känsligheten för insulin. Eller så är det något i själva fettlagringen som går snett när fettväven blivit för stor. Det är framförallt det sistnämnda som Olga Göransson håller på att studera närmare.
– Vi vill undersöka i detalj de basala mekanismerna för hur fett lagras hos friska och jämföra det med vad som händer i fettvävnad från överviktiga och insulinresistenta individer, säger Olga Göransson, forskare vid Medicinska fakulteten vid Lunds universitet.
Så pratar kroppen med cellen
Hennes specialområde är så kallad ”intracellulär signaltransduktion” eller hur yttre signaler kan prata med cellen, för att uttrycka det på ett enklare sätt. Signalmolekyler som kommer utifrån, t.ex. insulin från bukspottkörteln, kan oftast inte själva ta sig in i cellen och det behöver därför ske en signalöverföring för att insulinet och andra hormoner ska kunna påverka cellulära skeenden, t.ex. att socker tas upp från blodet.
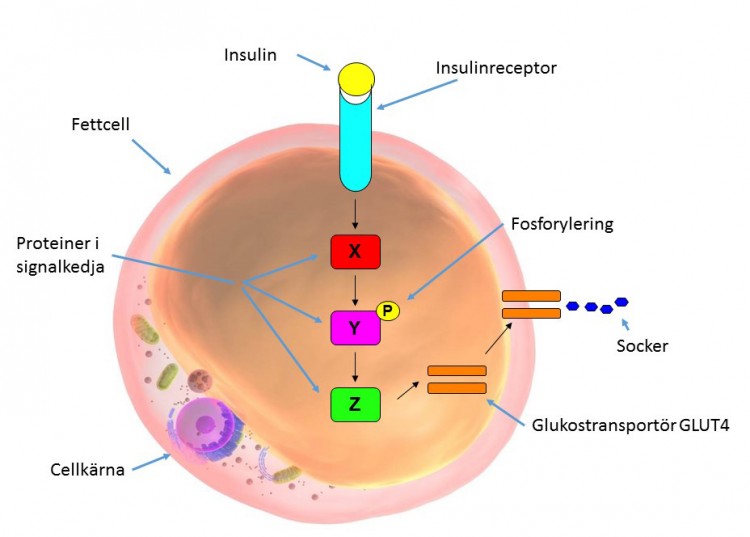
Signaler som kommer utifrån överförs via s.k. signalkedjor. Dessa består av olika proteiner som i tur och ordning påverkar varandra och på så sätt förs signalen framåt tills det ger upphov till ett biologiskt svar (se figur ovan). Här spelar proteinkinaser en viktig roll.
Proteinkinaser utgör själva länkarna i signalkedjan genom att fästa fosfatgrupper (små molekyler som innehåller fosfor) på nästa protein i signalkedjan. Fosfatgrupperna är en sorts ”på/av-knappar” som släpper fram signalen eller stoppar den.
Ett litet kinas kan vara skillnaden mellan frisk och sjuk fettvävnad
Olga Göransson och hennes forskargrupp har valt att studera några proteinkinaser i detalj för att ta reda på vilken roll de har vid fettlagring och hur de påverkas vid fetma. En av de mest intressanta just nu är kinaset SIK2 som förekommer i första hand i fettceller.
– Vi har kunnat visa att personer med fetma har generellt mindre av SIK2 jämfört med normalviktiga och att sambandet blir ännu tydligare om man jämför mängden SIK2 mot graden av insulinresistens. En del personer med fetma kan ändå ha ganska normala halter av SIK2 medan andra har alldeles för lite, men alla som är insulinresistenta har låga halter av SIK2. Kan det vara så att det är mängden SIK2 som skiljer metabolt friskt respektive sjukt fett och att SIK2 är nödvändigt för att behålla en normal insulinkänslighet?
I en tidigare studie kunde forskarna visa att SIK2 påverkar mängden av de glukostransportörer (GLUT4) som hjälper till att ta upp glukos (socker) från blodet (jfr figuren). Glukos behövs inte bara som en direkt energikälla för att upprätthålla kroppens olika funktioner utan även för att fettlagringen ska fungera normalt. SIK2 påverkar genuttrycket, dvs. hur aktiv genen för GLUT4 är. Ju högre koncentrationer av SIK2 desto större genuttryck, och desto fler GLUT4 som bildas.
I en pågående studie undersöker Olga Göransson och hennes kollegor bland annat om SIK2 även kan ha en mer direkt påverkan på själva signalkedjan, från insulin till GLUT4, och de effekter det skulle kunna få på glukosupptaget och kanske även fettomsättningen.
Vill hitta mål för behandling av insulinresistens
Olga Göranssons forskning går ut på att studera detaljerade processer som sker inne i cellerna, något vi inte kan se med blotta ögat men som ändå påverkar så många människors hälsa. Hur ser då framtiden ut, vad kommer man att veta om sambandet fetma och insulinresistens om tio år och hur kan de nya kunskaperna komma patienterna till nytta?
– Målet med vår forskning är att ta reda på om SIK2 kan utgöra mål för läkemedel för behandling av insulinresistens, säger Olga Göransson utan att tveka och fortsätter:
– Om man ser till forskarsamhällets samlade kunskap så tror jag att vi om tio år vet mycket mer om hur insulin styr fettlagring och om de främsta skillnaderna mellan frisk och sjuk fettväv. Jag hoppas också att vi har klarlagt vilken aspekt av fettvävsfunktionen som är viktigast för uppkomsten av insulinresistens. Är det fel i fettlagringen, obalans i fettvävshormonerna eller den låggradiga inflammationen? Eller en kombination av dessa tre?
Text: EVA BARTONEK ROXÅ
Foto (porträtt): ROGER LUNDHOLM