Tumörvävnadens styvhet spelar en roll för hur cancer sprider sig. Dessutom lämnar styv tumörvävnad spår i de drabbade cellerna. Detta visar två nya studier från Lunds universitet.
– Detta hjälper oss att bättre förstå hur de mekaniska egenskaperna i tumörens mikromiljö aktivt driver cancerutveckling och spridning, säger Vinay Swaminathan, forskare vid Lunds universitet.
Cancer sprider sig inte slumpmässigt i kroppen. Den fysiska miljön som omger en tumör består av ett nätverk av proteiner och sockerarter som kallas den extracellulära matrisen. Denna miljö spelar en aktiv roll för att avgöra om och hur cancerceller invaderar omgivande vävnad. Allteftersom tumörer utvecklas blir nätverket styvare och mindre flexibelt, det som känns som knölar vid bland annat bröstcancer.
Solida cancertumörer
En solid tumör är en fast, sammanhängande massa av cancerceller som växer i ett organ eller en vävnad. Den kallas solid eftersom den bildar en fysisk massa – till skillnad från till exempel blodcancer, som sprider sig via blodomloppet och inte bildar en solid tumör.
Den så kallade desmoplastiska ombyggnaden av tumörens mikromiljö – den onormala tillväxten av tät fibrös bindväv som omger en tumör och som ökar vävnadens styvhet – är ett vanligt inslag i många av de mest aggressiva cancerformerna, däribland bröstcancer, tjocktarms- och ändtarmscancer, bukspottkörtelcancer och lungcancer, där metastasering (spridning) fortfarande är den främsta orsaken till att behandlingen misslyckas och till dödsfall.
Att förstå hur celler reagerar på dessa fysiska förändringar ligger i skärningspunkten mellan teknik, fysik och biomedicin – kärnan i det område som kallas mekanobiologi, förklarar Vinay Swaminathan, universitetslektor vid Lunds universitet och ledare för forskargruppen Cellmekanobiologi.

– Man har länge misstänkt att fysiska förändringar i tumörmiljön får cancercellerna att bli mer aggressiva. Men de exakta molekylära mekanismerna, och huruvida effekterna kvarstår när den fysiska stimulansen upphör, har hittills inte varit helt klarlagda. Det är dessa frågor vi har försökt undersöka, säger Vinay Swaminathan.
Molekylära mekanismer bakom ökad invasivitet
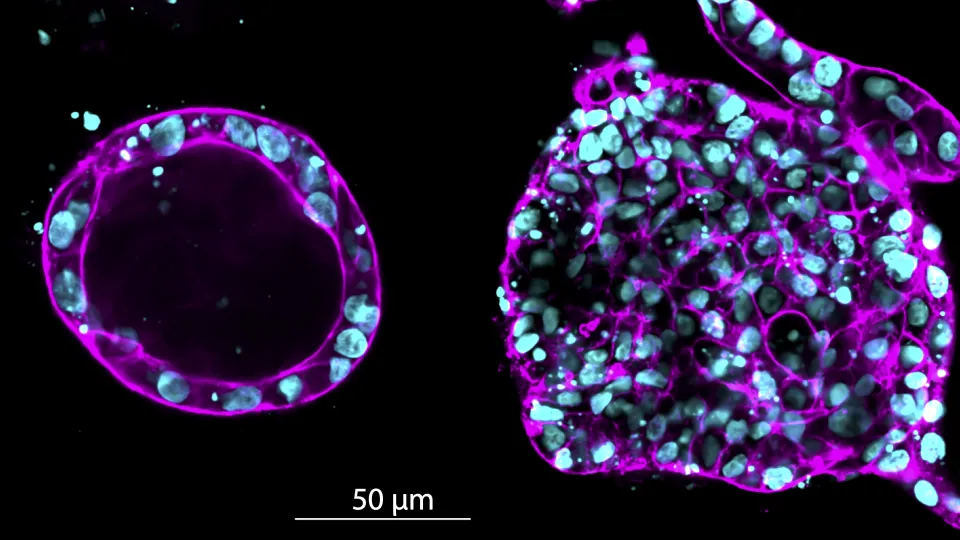
Båda studierna har publicerats i tidskriften Advanced Science. I den första studien undersöktes hur ökad styvhet i vävnadsmiljön utlöser cancerspridning. I laboratoriet utvecklade forskarteamet en exakt och kontrollerad 3D-modell med små kluster av bröstvävnadsceller – konstruerade att likna normal bröstvävnad. Cellerna odlades inuti en gel vars styvhet kunde justeras exakt, utan att cellerna själva stördes.
– Med hjälp av detta system upptäckte vi att när den omgivande vävnaden stelnar sätts en specifik kedja av molekylära händelser i gång”, säger biträdande forskaren Kabilan Sakthivel, som ledde studien.
Forskarna identifierade en kedja av tre proteiner som driver denna process: β1-integrinet på cellytan aktiverar signalproteinet FAK, som i sin tur aktiverar Piezo1, en mekanokänslig jonkanal. Tillsammans får dessa proteiner cellerna att ändra form och tränga in i den omgivande vävnaden.

– Avgörande är att när vävnaden mjukades upp igen efter att ha stelnat, vändes invasionen – vilket tyder på att tidpunkten spelar en enorm roll. Om man ingriper tillräckligt tidigt kan processen återställas till det normala. Men det verkar finnas en punkt där det inte längre går att vända utvecklingen: Detta gör de tidiga mekaniska förändringarna i tumörvävnaden till ett potentiellt viktigt behandlingsfönster, säger Kabilan Sakthivel.
Bestående förändringar i stödjeceller
Den andra studien fokuserade på fibroblaster – stödceller som omger tumörer och bidrar till att vävnaden blir styvare. Långvarig exponering för en styv miljö fick dessa celler att permanent övergå till ett aktiverat tillstånd som främjar tumörtillväxt, en effekt som kvarstod även när cellerna återfördes till en mjuk miljö.
– Denna bestående förändring berodde inte på en genetisk mutation, utan på förändringar i hur cellens genetiska information är fysiskt organiserad i cellkärnan – en process som kallas epigenetisk omprogrammering, säger doktorand Swathi Packirisamy, som ledde den andra studien.
Forskarna identifierade två parallella molekylära signalvägar som ligger bakom denna omprogrammering, vilka båda leder till en komprimering av kromatinet som håller cellerna kvar i ett aktiverat tillstånd. Det räckte med att blockera endera av dessa signalvägar för att förhindra övergången – och celler som redan hade påverkats kunde återställas till sitt normala tillstånd.
– Det som fascinerar mig mest är att det här handlar om grundläggande biologi – att förstå hur celler tolkar och lagrar information om sin fysiska omgivning på molekylär nivå. Men eftersom vi nu kan identifiera specifika punkter i denna kedja där processen kan avbrytas eller vändas, finns det en konkret väg från dessa grundläggande upptäckter till nya behandlingsstrategier”, säger Vinay Swaminathan.
Länkar till publikationer
Integrin-Piezo1 Axis Drives ECM Remodeling and Invasion of 3D Breast Epithelium
Text: ERIKA SVANTESSON
Artikeln är tidigare publicerad som nyhet från Lunds universitet

