Det senaste decenniet har kunskapen om hur våra gener påverkas av vår livsstil – ett forskningsfält som kallas epigenetik – ökat explosionsartat. Forskare vid Lunds universitets Diabetescentrum har sammanfattat det vetenskapliga kunskapsläget inom epigenetik kopplat till fetma och typ 2-diabetes i en översiktsartikel.
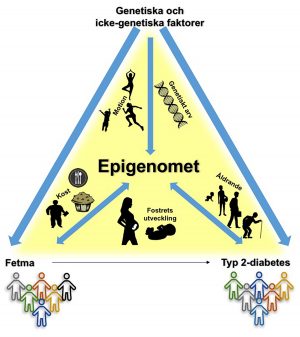
Epigenetiska mekanismer (se faktaruta) kontrollerar aktiviteten i olika gener. Störningar i dessa kan leda till sjukdomar som bland annat fetma och typ 2-diabetes. Den här översikten summerar vilken roll som förändringar i epigenetiska mönster har i olika kroppsvävnader som är av betydelse för ämnesomsättningen, exempelvis i fettväv, skelettmuskulatur, langerhanska öar (som bland annat innehåller de insulinproducerande cellerna), lever och blod, kopplat till fetma och typ 2-diabetes.

– Epigenetik är fortfarande ett ungt forskningsfält, men vi vet idag att epigenetiska mekanismer har betydelse för sjukdomsutvecklingen. Likaså påverkas de epigenetiska mönstren av sjukdom. Variationer i arvsmassan (DNA), ålder, träning och kost bidrar också till epigenetiska variationer, säger Charlotte Ling, professor och pionjär inom fältet epigenetik och diabetes som tillsammans med forskaren Tina Rönn författat översikten.
Här sammanfattas de senaste rönen inom respektive kategori:
Kostens betydelse
Forskning visar att kosten påverkar epigenomet i flera vävnader som är viktiga för ämnesomsättningen. Artikelförfattarna skriver att det gjorts flera interventionsstudier (då man delat in deltagare i grupper med varierande kosthållning efter olika principer då man studerat olika dieters effekt på epigenomet). Några exempel:
- Fettrik kost under fem dagar ledde till både ändrad genaktivitet och DNA-metyleringsmönster i skelettmuskulatur och fettväv.
- Mättat eller fleromättat? I en studie fick deltagarna under sju veckor äta muffins som bakats med antingen mättat eller fleromättat fett. Alla deltagarna gick upp lika mycket i vikt, men de som åt mycket mättat fett drabbades i högre utsträckning av bukfetma och lagrade sitt fett i levern. DNA-metyleringen i fettväven skilde sig också åt mellan de båda grupperna.
– Både bukfetma och fett som lagras i exempelvis muskler och lever är riskfaktorer för diabetes och hjärt-kärlsjukdomar. En annan viktig iakttagelse var att det verkade enklare att öka antalet metyleringsförändringar genom att äta en fettrik kost än att senare bli av med dem med hjälp av en kontrollerad kost, säger Charlotte Ling.
Fysisk aktivitet

Det är väl känt att regelbunden träning förebygger och förhindrar att personer med hög risk för typ 2-diabetes utvecklar sjukdomen. Motion har positiva effekter på sockeromsättningen och hela kroppens energibalans, liksom på immunförsvaret.
Artikelförfattarna beskriver flera studier som visat att träning påverkar DNA-metylering (se faktaruta) och genernas funktion i skelettmuskulatur och fettväv.
- En studie från 2013 visar att epigenetiska förändringar som uppstår under träning påverkar omsättningen av fettsyror i fettväv genom att öka aktiviteten i specifika gener.
- Motion under kortare eller längre tid har en tydlig påverkan på DNA-metylering och detta skiljer sig åt mellan både gener och vävnader.
– Epigenetik kan förklara varför olika människor svarar olika på träning, säger Tina Rönn.
Åldrande
Åldrande är kopplat till ökad bukfetma, insulinresistens och typ 2-diabetes. En ökad förståelse för de åldersrelaterade mekanismerna som leder till fetma och typ 2-diabetes kan därför leda till nya och förebyggande behandlingsmetoder.
Forskningen visar att:
- Åldrandeprocessen präglas av större variation i epigenomet i och med att generna förlorar eller förvärvar nya metyleringar.
- Fetma verkar ha en inverkan på åldersframkallade epigenetiska förändringar vilket kan innebära att det finns en molekylär länk mellan åldrande och fetma.
– Även om DNA-metylering är en stabil epigenetisk markör, vet vi att epigenomet ändras över tid, säger Charlotte Ling.
Genernas betydelse
Våra gener styrs i en extremt komplex process som startar i genens molekylära byggstenar, de så kallade nukleotiderna, som bygger upp strängen av DNA. Lägg sedan till DNA-metylering, RNA-molekyler och histon-modifikationer (kemiska grupper som binder till och påverkar de proteiner kring vilka vår långa DNA-spiral är uppsnurrade), som alla också påverkas av både genetiska och miljömässiga faktorer.
Studier visar att:
- Eftersom DNA-metylering huvudsakligen äger rum på specifika ställen i vårt DNA, kan ärftliga variationer i genernas sammansättning påverka möjligheten för metylgrupperna att alls fästa till generna.
- En studie på de så kallade langerhanska öar från bukspottkörteln visar att hälften av alla genvarianter som kan kopplas till typ 2-diabetes också skapar eller tar bort ställen där DNA-metylering kan ske, varav en del av dessa även kunde kopplas till genernas funktion och cellernas förmåga att utsöndra insulin.
- Olika genvarianter kan reglera effekten på metabola tillstånd såsom BMI (Body Mass Index) och HbA1C genom skillnader i mängden DNA-metylering.
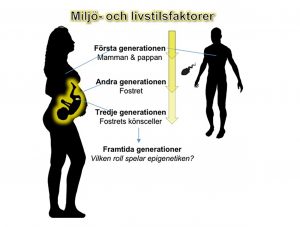
Kan man ärva epigenomet?
Det är en spännande och utmanande tanke att epigenetisk ärftlighet bidrar till evolutionen, skriver författarna. Epigenomet är föränderligt, och kan anpassa sig fortare till de senaste decenniernas stora förändringar i vår livsstil än vad våra gener hinner ändras till följd av mutationer. Under fosterstadiet sker den mest aktiva epigenetiska programmeringen av fostrets gener. Artikelförfattarna beskriver att det en kvinna utsätts för under graviditeten inte bara påverkar henne själv och hennes ofödda barn, det påverkar även hennes barnbarn genom att det präglar fostrets egna könsceller. Både ägganlag och det som senare ska bli spermier bildas redan under fosterstadiet och utgör delar av arvsmassan inuti könscellerna.
– För att kunna belägga att epigenetiska förändringar kan ärvas mellan flera generationer, måste man ha kunnat påvisa förändringar även i den fjärde generationen, och vad vi vet finns det idag bara svaga bevis för att epigenetiska förändringar ärvs mellan generationer mellan människor, berättar Tina Rönn.
Det publiceras nu allt fler studier om överföringen av epigenetisk information från pappan. Bland annat har man sett att även spermier har ett epigenom som påverkas av omgivningsfaktorer och som sannolikt har en påverkan på nästa generation:
- Bland annat visar en studie från 2016 att DNA-metylomet i spermier från fetmaopererade män, som genomgått bariatrisk kirurgi, ändrades efter operationen.
- Även träning har förmågan att ändra metylomet i spermier, har en tidigare studie visat, men huruvida dessa förändringar ärvs och är till nytta för barnen är oklart.
Hur kan epigenetik bidra till nya behandligar?
Det är sedan tidigare känt att regelbunden motion och hälsosam kost kan förhindra att individer i riskzonen för typ 2-diabetes utvecklar sjukdomen. Det är därför viktigt att tidigt kunna identifiera dessa individer.
- Epigenetiska markörer kan i framtiden bli möjliga att använda för att förutse vem som löper hög risk att drabbas av fetma och typ 2-diabetes, under förutsättning att de är lätta att mäta, som exempelvis i blod, skriver artikelförfattarna.
- Nya teknologiska metoder som gör det möjligt att rikta läkemedel mot ett specifikt mål kan ge oss möjlighet att utveckla nya behandlingsmetoder. Dessa skulle kunna riktas mot epigenetiska förändringar eftersom dessa kan ändras.
Det finns redan läkemedel som har effekt på DNA-metylering och histonmodifiering. Dessa har testats med goda resultat vid exempelvis leukemi. Författarna menar att epigenetiska läkemedel även skulle kunna ha effekt vid fetma och typ 2-diabetes då studier i flera fall visat att de förbättrar insulinsekretion.
– Eftersom typ 2-diabetes är en kronisk sjukdom skulle det behövas livslång medicinering och man måste därför väga fördelar mot nackdelar och studera eventuella biverkningar först, säger Charlotte Ling.
FAKTA Epigenetik
I kroppens celler finns vår arvsmassa, DNA, som innehåller gener. Generna ärver vi och de kan inte ändras. DNA-metylering är den del i epigenetiken som utforskats mest (och som denna översikt handlar om) och innebär att kemiska föreningar, så kallade metylgrupper, sätter sig på generna vilket påverkar deras funktion.
Då de första studierna inom epigenetik och typ 2-diabetes gjordes för drygt tio år sedan analyserades DNA-metyleringar på utvalda kandidatgener eller små delar av arvsmassan. Med senare teknik blev det möjligt att analysera arvsmassans samtliga gener i dess minsta beståndsdelar där metyleringarna sitter, så kallade CpG-sites. I dag går det att studera hela epigenomet med en teknik som heter ”hel-genom-bisulfit-sekvensering” (WGBS), då analyseras DNA metylering över 80 procent av alla CpG-sites i hela arvsmassan (genomet). Epigenomet inkluderar förutom DNA-metylering även olika histonmodifikationer och små icke-kodande RNA.
Vetenskaplig publikation: Epigenetics in human obesity and type 2 diabetes
Text: SARA LIEDHOLM
Illustration kromosom: iStock/blackjack3D
Artikeln är tidigare publicerad som nyhet från Lunds universitet