”Snälla” bakterier gör oss sällan sjuka – men kan göra det under vissa omständigheter. ”Elaka” bakterier gör oss ofta sjuka – men inte alltid. Varför är det så?
Pontus Nordenfelt menar att det beror på den lokala mikromiljön som bakterien befinner sig i. Han forskar inom infektionsmedicin vid Lunds universitet och har döpt sin forskargrupp till ”Kvantitativ infektionsbiologi”. Det avspeglar tydligt vad som ligger i fokus för hans forskning.

– Tidigare forskning har i huvuddrag velat beskriva vilken eller vilka molekyler som gör en bakterie patogen, det vill säga sjukdomsalstrande. Jag tror att det också är viktigt att besvara exempelvis frågan hur många molekyler som krävs för att den ska orsaka sjukdom. Jag vill kunna mäta och sätta siffror på saker och ting – det vill säga kvantifiera – för att få en mer detaljerad bild av vad som är viktigt och när.
Närmiljön avgör
Ett sådant exempel är bakterien Streptococcus pyogenes, en så kallad grupp A-streptokock som kan orsaka både den mildare sjukdomen halsfluss men också mycket allvarliga tillstånd som sepsis eller allvarlig mjukdelsinfektion, ibland kallad köttätande sjukdom, då bakterier ”äter sig in” i bindväven. Faktum är att många i befolkningen kan bära på den här bakterien i halsen utan att alls bli sjuka.
För några år sedan publicerade Pontus Nordenfelt och hans kollegor resultat som visade att bakteriernas förmåga att orsaka sjukdom var beroende av antikroppskoncentrationen i deras närmiljö. De kunde visa att ute i vävnader, som till exempel i halsen, där antikroppskoncentrationen är låg, sitter antikropparna felvända på bakteriens yta. Det gör att immunförsvaret inte känner igen dem som inkräktare. Här har alltså halsflussbakterien utvecklat ett sätt att samexistera med oss människor utan att ställa till med några större besvär. Om samma bakterie lyckas ta sig ut till blodet, där antikroppskoncentrationen är hög, binder antikropparna rättvänt och aktiverar immunförsvaret. Ibland lyckas försvaret med att ta död på bakterierna men ibland blir reaktionen så kraftig att det leder till livshotande tillstånd som köttätande sjukdom eller sepsis.
Första mötet viktigt
Den lokala mikromiljön är viktig, men även det lokala mötet mellan bakterie och människocell. Och det är det sistnämnda som är i fokus för Pontus Nordenfelts forskning just nu – att beskriva det första mötet mellan bakterie och människocell.
Han är speciellt intresserad av integriner. Det är molekyler som finns på ytan av våra celler och som cellen använder för att interagera med sin omgivning, bland annat för att fästa på ytor och flytta på sig. Bakterier å sin sida kan använda sig av integriner som handtag för att klamra sig fast på ytor i kroppen så att de inte spolas bort eller för att ta sig in i människoceller.
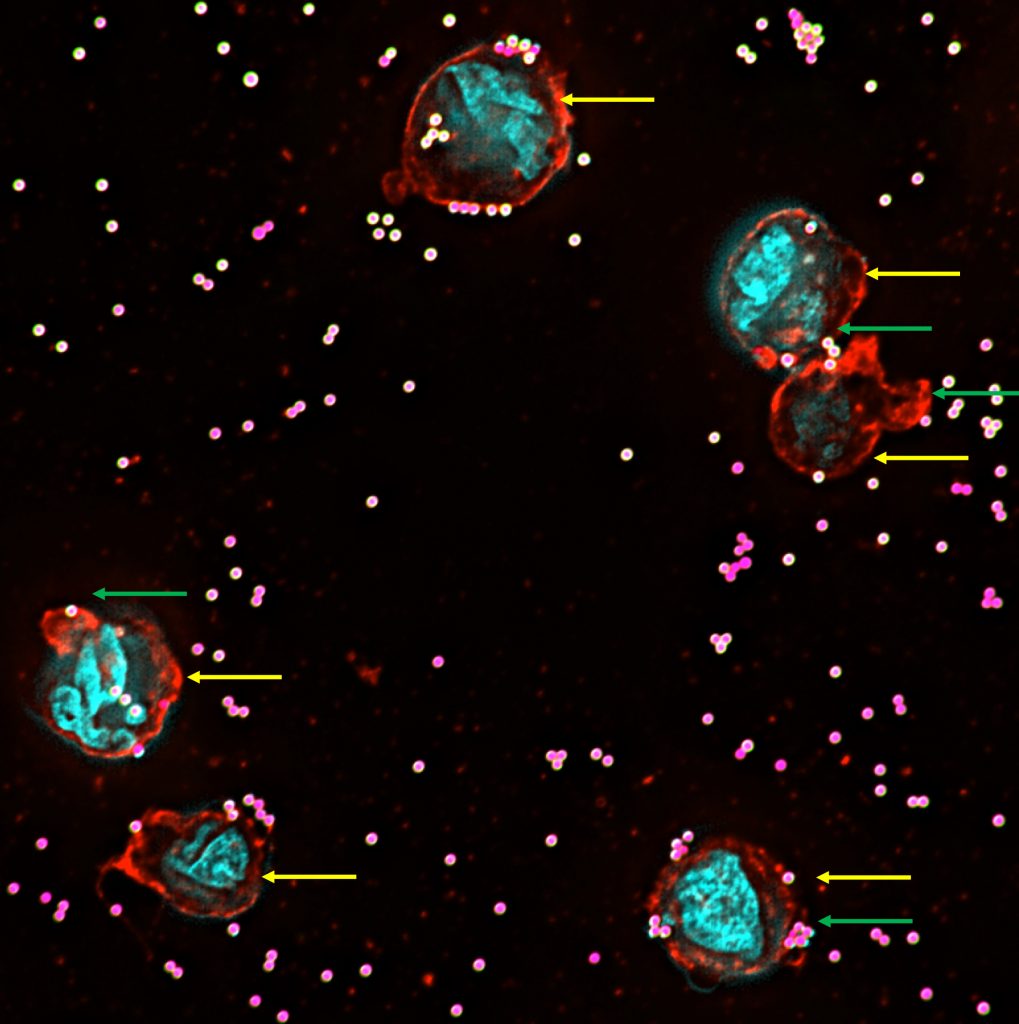
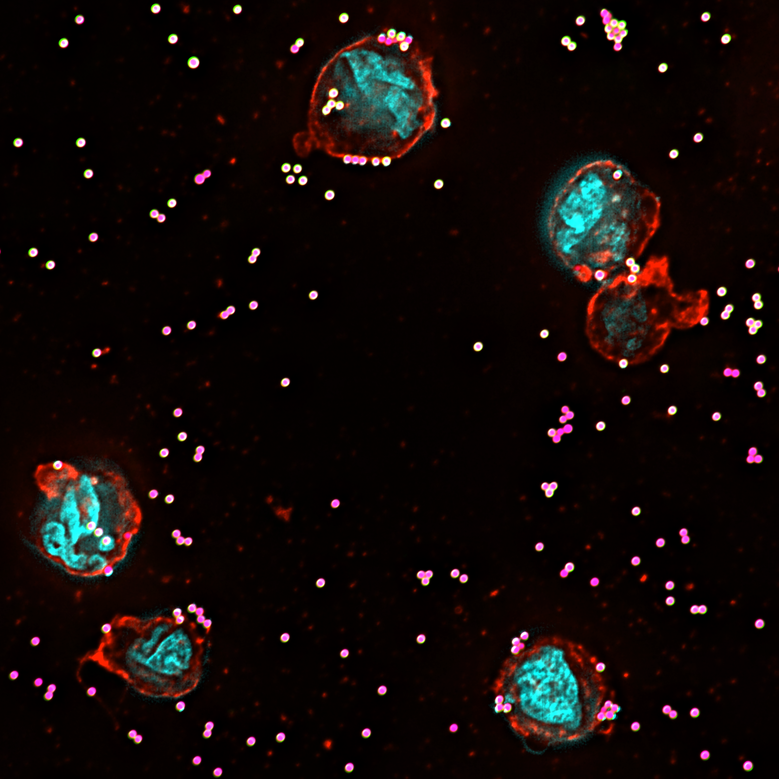 Nytt mikroskop ska avslöja första mötet
Nytt mikroskop ska avslöja första mötet
– Just nu håller vi på att utveckla tekniken. Vi bygger avancerade mikroskop för att kunna studera det första mötet mellan bakterie och människocell in i minsta detalj. Många bakterier har som strategi att ”klä sig” med mänskliga proteiner, som integriner sedan gärna binder till. När tekniken är på plats hoppas vi kunna besvara frågor om vilka proteiner som integrinerna aktiveras av, hur snabbt de aktiveras och inte minst hur många molekyler som krävs för en aktivering.
På sikt hoppas Pontus Nordenfelt och hans forskagrupp kunna bidra till en bättre förståelse av de molekylära mekanismerna som triggar igång sepsis.
– Jag hoppas att vi ska kunna bidra med ny kunskap om vilka molekyler, och i vilka mängder, som är viktiga. Då kan vi till exempel peka ut för läkemedelsindustrin vilka molekyler de ska fokusera på vid utvecklingen av läkemedel mot sepsis, säger Pontus Nordenfelt.
Och drömmen på lång sikt är att hitta generella mekanismer som sjukdomsalstrande bakterier använder sig av för att häfta vid och invadera våra celler. Sådan kunskap skulle kunna öppna upp för bättre diagnostik och behandling av infektioner i allmänhet.
Text: EVA BARTONEK ROXÅ
Lär dig känna igen symtom vid sepsis